Institut

Grundsätze
Präzise, zügige und verständliche Diagnostik.
Die MVZ Prof. Dr. med. A. Niendorf Pathologie Hamburg-West GmbH bietet exakte und schnelle Befundung durch erfahrene Fachärzte, die sich an vorgegebenen Kriterien und Leitlinien orientiert. Karzinomdiagnosen werden grundsätzlich einer Doppelbefundung unterzogen.
Im Sinne eines effizienten Qualitätsmanagements überprüfen wir eigene Diagnosen mit statistischen Mitteln und führen regelmäßig retrospektive Follow-up Untersuchungen durch. In Bedarfsfällen konsultieren wir jederzeit renommierte Gutachter aus einem Netzwerk internationaler Kollegen.
Unser besonderes Augenmerk gilt der individuellen Beratung und dem partnerschaftlichen Austausch mit Kollegen im stationären und ambulanten Bereich. Zu aktuellen Themen bieten wir regelmäßige Informations- und Fortbildungsveranstaltungen.
Angehende Fachärzte können in unserer Praxis ihre Weiterbildung abschließen.
Die Basis für Therapien in der Onkologie
Lernen Sie die Pathologie kennen
Ihr zuverlässiger Partner in der Pathologie
Lernen Sie unser Team kennen
Geschäftsführung
Ärzte

Prof. Dr. med. Axel Niendorf
Histologische Diagnostik
Zytologische Diagnostik

PD Dr. med. Axel Greiner
Histologische Diagnostik

Sebastian Fehr
Histologische Diagnostik

Dr. med. Sonja Herbst
Histologische Diagnostik
Ärzte in Weiterbildung
Fachliche Vernetzung
Kooperationen und Mitgliedschaften
Unsere erfahrenen Pathologen sind Mitglieder in verschiedenen Fachgesellschaften. Teilnahmen an Jahrestagungen und Kongressen sind bei uns eine Selbstverständlichkeit, um Wissen und Erfahrungen auszutauschen und zu mehren.
Kliniken
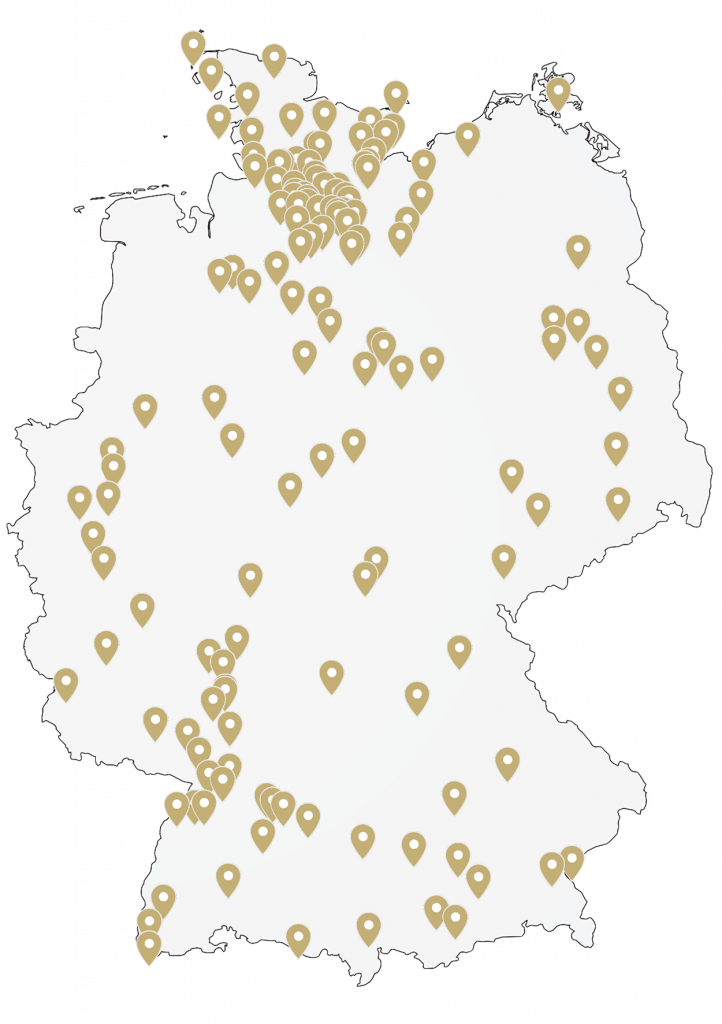
Ambulante Praxen in ganz Deutschland
Sana Kliniken Lübeck
BG Klinikum Hamburg
Bethesda Krankenhaus Bergedorf
Helios Mariahilf Klinik Hamburg
Klinik Dr. Guth Hamburg
Krankenhaus Tabea Hamburg
WKK
Heide
WKK
Brunsbüttel
Fachliche Vernetzung
Forschung
Publikationen
Gasior A, Wegscheider A-S, Paveley J, Howard K J, Harrison M,Gough L, Gorniak J, Rollinson S, Pounce Z, Niendorf A
Enhancing HER2 evaluation: Correlation of APIS Breast Cancer Subtyping Kit and IHC/ISH with accurate HER2 quantification.
2024 Juni DOI: 10.1200/JCO.2024.42.16_suppl.e13028
Gasior A, Gorniak J, Rollinson S,Gough L,Wegscheider A-S, Niendorf A
Abstract PO1-02-08: Comprehensive Molecular Profiling of Breast Cancer: A real-time PCR assay for identifying ESR1, PGR, ERBB2, MKI67 and a novel proliferative signature in core needle biopsies and resected invasive breast cancer tissues
2024 Mai DOI: 10.1158/1538-7445.SABCS23-PO1-02-08
Wegscheider A-S, Wojahn I, Gottheil P, Spohn M, Käs J A, Rosin O, Ulm B, Nollau P, Wagener C, Niendorf A, Wolters-Eisfeld G
CD301 and LSECtin glycan-binding receptors of innate immune cells serve as prognostic markers and potential predictors of immune response in breast cancer subtypes
2024 Jan. DOI: 10.1093/glycob/cwae003
Tschodu D, Lippoldt J, Gottheil P, Wegscheider A-S, Käs J A, Niendorf A
Re-evaluation of publicly available gene-expression databases using machine-learning yields a maximum prognostic power in breast cancer
2023 Oct. DOI:10.1038/s41598-023-41090-9
Wegscheider A-S, Tauber N, Graubner K, Ziegeler G, Behr M, Lindner C, Niendorf A
Synchronous High-Grade Squamous Intraepithelial Lesion of the Fimbria of the Fallopian Tube in a 51-Year-Old Woman with Invasive Squamous Cell Carcinoma of the Uterine Cervix
2023 Sep. DOI: 10.3390/diagnostics13172836
Webersinke G, Burghofer J, Malli T, Rammer M, Wenzel jahn S, Niendorf A, Tavassoli F A, Moinfar F:
TERT Promoter Mutation c.-124C>T Commonly Occurs in Low-Grade Fibromatosis-like Metaplastic Breast Carcinoma
2023 March DOI: 10.5858/arpa.2022-0159-OA
Desmoid Type Fibromatosis of the Breast: Ten-Year Institutional Results of Imaging, Histopathology, and Surgery
Fritz P, Bendrat K, Sonnenberg M, Trautmann C, Ott G, Heidemann E, Brinkmann F, Faisst S, Gerteis A, Brauch H, Schwab M, Lindner C, Friedrichs K, Alscher MD, Dippon J, Niendorf A:
Tubular breast cancer. A retrospective study.
Anticancer Research, 2014, 34(7), pp. 3647-56
Khosrawi P, Bollweg L, Niendorf A, Sailer M:
Unklarer Milztumor bei Rektumkarzinom
Der Chirurg, 2014, 85(12), pp. 1094-1096
Nollau P, Wolters-Eisfeld G, Mortezai N, Kurze AK, Klampe B, Debus A, Bockhorn M, Niendorf A, Wagener C:
Protein domain histochemistry (PDH): binding of the carbohydrate recognition domain (CRD) of recombinant human glycoreceptor CLEC10A (CD301) to formalin-fixed, paraffin-embedded breast cancer tissues.
Lindner C, Gieseking F, Niendorf A:
Gebärmutterhalskrebs heilen und verhindern.
Hamburger Ärzteblatt 2013, 11, pp. 12-17
Recognition of glykan-epitopes by the macrophage glycoreceptor CLEC10A is associated with improved outcome in primary breast cancer.
Cancer Res 2013, 73 (24 Suppl), Abstract no. P3-05-14.
Microscopes and beyond--advanced pathology
A compartment-specific transcriptome analysis reveals survival-relevant marker genes in the stroma fraction of squamous non-small cell lung cancer
Sensor-based cell and tissue screening for personalized cancer chemotherapy
Medical and Biological Engineering and Computing, 2012, 50(2), pp. 117-126
Das Ligamentum-coracoacromiale-Regenerat – eine histologische Studie
Orthopädische Praxis, 2011, 47(1), pp. 9-17
A new method for histological microdissection utilizing an ultrasonically oscillating needle: demonstrated by differential mRNA expression in human lung carcinoma tissue
Detection and quantification of lipoprotein(a) in the arterial wall of 107 coronary bypass patients Abstract
Gottheil P, Lippoldt J, Grosser S, Renner F, Saibah M, Tschodu D, Poßögel AK, Wegscheider AS, Ulm B, Friedrichs B, Lindner C, Engel C, Löffler M, Wolf B; Höckel M, B Aktas B, Kubitschke H, Niendorf A, Käs JA:
State of Cell Unjamming Correlates with Distant Metastasis in Cancer Patients
Comparative analysis of molecular signatures reveals a hybrid approach in breast cancer: Combining the Nottingham Prognostic Index with gene expressions into a hybrid signature
Altona Prognostic Index: A New Prognostic Index for ER-Positive and Her2-Negative Breast Cancer of No Special Type
Felix Wiedbrauck, Martin Keuchel, Axel Greiner,
Jörg Caselitz, Yasuo Kakugawa, and Yutaka Saito
Malignant Tumours
Fachliche Vernetzung
Projekte

GlyCan-Projekt
Initiatoren
Pathologie Hamburg-West / Prof. Wagener und Dr. Nollau (Universitätsklinikum Hamburg-Eppendorf)
Das Acronym „GlyCan“ vereint die beiden Schlüsselbegriffe dieses Projekts, „Glycans“ und „Cancer.“
Ziel dieses Projektes ist es, die Zusammensetzung der Zuckerverbindungen (Glykane) auf der Oberfläche von Tumorzellen genau zu untersuchen und Muster zu finden, die spezifisch nur auf bestimmten Tumoren gefunden werden. Am Projektende soll ein Testkit entwickelt werden mit dem es möglich sein wird, einen Tumor anhand seines spezifischen Glykanmusters genau zu identifizieren.

PAtepo-Projekt
Initiatoren
Pathologie Hamburg-West / TILL I.D. GmbH / Ludwig-Maximilians-Universität München
Das Verbundprojekt PaTePo wurde gemeinsam mit der TILL I.D. GmbH und der Ludwig-Maximilians-Universität in München initiiert.
Das Akronym PaTePo setzt sich aus den Wörtern Pathologie und Teleportation zusammen und steht für das Vorhabenziel, durch innovative Technologie und ein entsprechendes Training vor Ort eine ortsaufgelöste Beurteilung von im Rahmen von Schnellschnitten entnommenen Gewebeproben durch einen Facharzt für Pathologie zu ermöglichen.

ExprImage-Projekt
Initiatoren
Universitätsklinikum Hamburg-Eppendorf / Universität Jena / Universität Leipzig / Fraunhofer / Institut für angewandte Informationstechnik FIT / Zeiss / Qiagen / Witec GmbH
Das Kunstwort „ExprImage“ vereint die beiden Schlüsselbegriffe des Verbundprojekts, „Expression“ und „Image.“
Ziel ist die Generierung einer Hybridsignatur unter Berücksichtigung von Morphologie und molekularen/proteomischen Biomarkern bzw. die Entwicklung einer multidimensionalen Tumorpathologie durch eine integrierte Auswertung von histologischen Bilddaten, molekularbiologischen Expressionsdaten sowie weiterer klinischer Parameter, die eine verbesserte Einschätzung von individueller Prognose und optimaler Therapieoption ermöglicht.
















